今天推荐的是由武汉大学公共卫生学院、郑州大学附属肿瘤医院等单位合作,于2026年3月发表于Advanced Science的研究论文。该研究通过对482例胰腺组织进行大规模eQTL(表达数量性状位点)荟萃分析,构建了胰腺癌遗传调控图谱,并整合GWAS数据,系统鉴定了82个功能性变异和15个靶基因。研究重点揭示了rs11102484位点通过等位基因依赖的远距离沉默子-启动子互作,调控ST7L表达,进而影响AKT/β-catenin信号通路和胰腺癌风险的完整机制。这项工作为理解非编码区风险变异的生物学功能提供了范式,并为胰腺癌的精准预防和治疗开辟了新方向。实验中所使用的细胞系均是由苏州鉴达生物科技有限公司(Genetic Testing Biotechnology)通过STR分型技术进行的身份鉴定,确保了实验所用细胞的来源可靠与身份准确。
研究背景
胰腺癌是恶性程度最高的实体肿瘤之一,五年生存率不足10%,其早期诊断困难、预后极差。全基因组关联研究(GWAS)已鉴定出多个胰腺癌风险位点,但超过90%的风险变异位于非编码区,且由于连锁不平衡的干扰,从中识别因果变异及其靶基因极为困难。传统的表达数量性状位点(eQTL)分析可建立遗传变异与基因表达的关联,但既往研究受限于胰腺组织样本量小、缺乏功能验证,导致“变异-基因-疾病”的完整因果链长期未能阐明。如何系统性地从GWAS信号中筛选出真正具有调控功能的变异,并将其与下游靶基因及信号通路连接,是该领域的核心挑战。
摘要部分
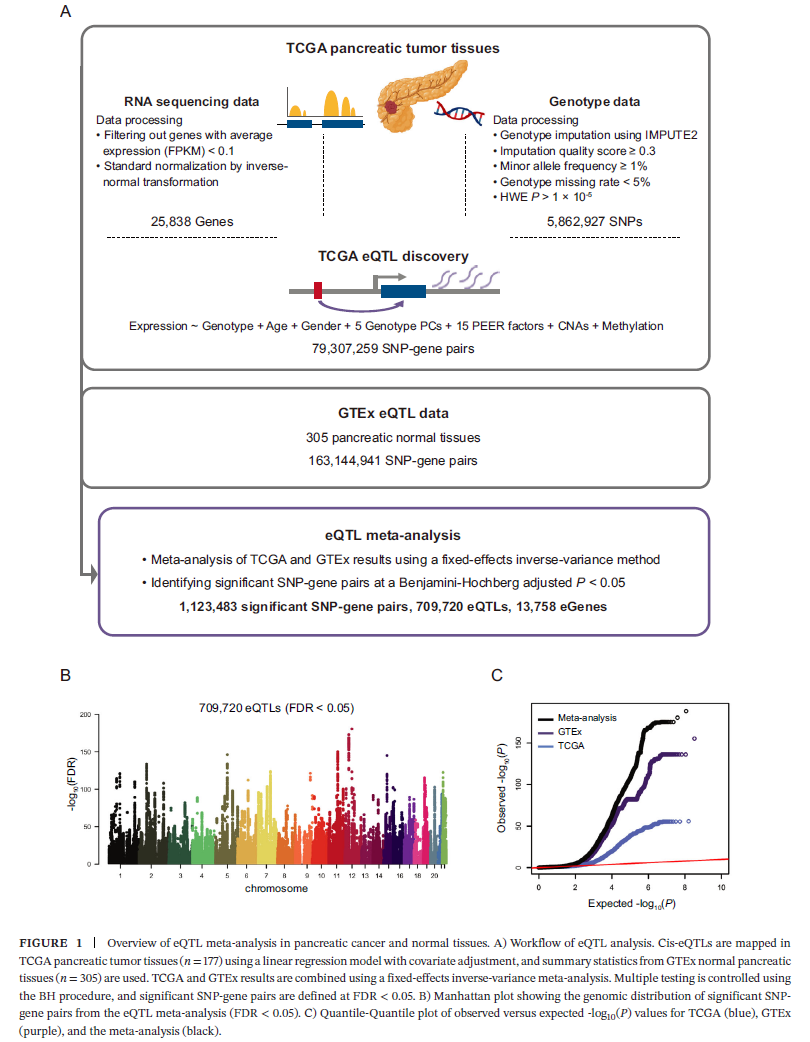
本研究整合了TCGA(177例胰腺癌组织)和GTEx(305例正常胰腺组织)的转录组与基因组数据,通过固定效应荟萃分析,鉴定出超过70万个独特的eQTL,覆盖13,758个eGenes(包括蛋白编码基因、lncRNA和假基因)。这些eQTL显著富集于开放染色质区域、活性组蛋白修饰区以及转录因子(如POLR2A、MYC、YY1)和RNA结合蛋白的结合位点。进一步将eQTL与包含5,130例病例和5,776例对照的GWAS荟萃分析结果整合,优先筛选出82个功能性变异和15个候选易感基因。其中,rs11102484(1p13.2)表现出最强的调控潜力。通过独立队列(569例病例,2,691例对照)验证,rs11102484的G等位基因与胰腺癌风险显著降低相关(OR=0.85,P=4.83×10⁻⁸)。机制研究表明,G等位基因破坏了转录抑制因子ZNF263与沉默子区域的结合,从而减弱了该位点与ST7L启动子之间的远距离染色质环互作,导致ST7L表达上调。升高的ST7L通过抑制AKT磷酸化和β-catenin信号,显著抑制胰腺癌细胞增殖。本研究系统解析了胰腺癌遗传易感性的调控网络,揭示了rs11102484-ST7L轴作为潜在治疗靶点的价值。
研究内容
构建胰腺组织高分辨率eQTL图谱
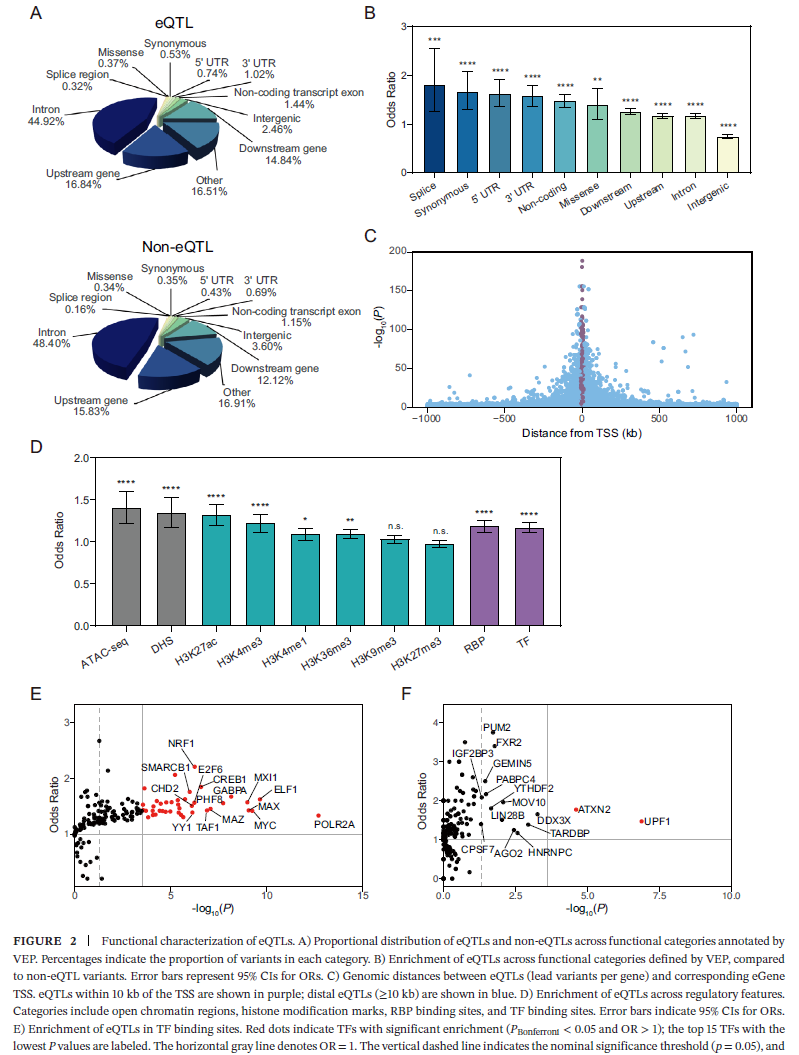
研究团队首先对482例胰腺组织样本(177例肿瘤+305例正常)进行cis-eQTL荟萃分析,共识别出1,123,483个显著的SNP-基因对,对应709,720个独特eQTL和13,758个eGenes。与单队列分析相比,荟萃分析显著提高了统计功效,并扩展了对非编码基因(如lncRNA)的调控发现。这些eGenes中,蛋白编码基因占10,304个,lncRNA达2,460个,反映了广泛的调控景观。
功能注释显示,eQTL显著富集于内含子区、5'/3'UTR区,而在基因间区显著缺失。此外,eQTL在ATAC-seq和DNase-seq定义的开放染色质区域、H3K27ac/H3K4me1/H3K4me3等活性组蛋白修饰区域中高度富集,而抑制性修饰(H3K9me3、H3K27me3)无显著富集。特别值得注意的是,eQTL显著富集于多个癌症相关转录因子的结合位点,如POLR2A、MYC、YY1和ELF1,这些因子此前已被报道参与胰腺癌进展。
eGenes的生物学与临床意义:从通路富集到药物响应
对13,758个eGenes进行通路富集分析,发现它们显著富集于DNA修复、脂肪酸代谢、mTORC1信号和p53通路等癌症相关通路。在1062个文献报道的胰腺癌相关基因集中,eGenes显著过表达(P=1.22×10⁻⁶⁶)。TCGA体细胞突变分析显示,eGenes覆盖了KRAS(74%)、SMAD4(71%)、TP53(61%)等经典驱动基因,88.11%的胰腺癌样本至少携带一个eGenes的突变或拷贝数变异。
免疫浸润分析表明,大量eGenes的表达与巨噬细胞、CD8⁺ T细胞和髓系树突状细胞的丰度显著相关。例如,SLC8A1与巨噬细胞浸润高度相关,ANO6与多种免疫细胞群体相关。此外,通过GDSC数据库分析,研究发现了大量eGene-药物敏感性关联,其中PI3K/mTOR信号通路相关的eGene数量最多。这提示eGene表达谱有潜力作为预测药物响应的生物标志物。
eQTL-GWAS整合:优先筛选82个功能性变异与15个易感基因
研究团队将胰腺eQTL数据与两项GWAS(PanC4和中国人群)的荟萃分析结果进行整合。GWAS荟萃分析共纳入5,130例病例和5,776例对照,鉴定出183个候选SNP(Pmeta<1×10⁻⁵,且两人群均P<0.05)。通过与eQTL取交集,最终获得82个同时与胰腺癌风险和基因表达显著关联的功能性SNP,映射到15个候选基因(如ETAA1、GSDMB、PDX1、ST7L等)。这些基因显著富集于致癌特征基因集以及AGE/RAGE、IL-1、TNF-α等信号通路。
利用多种计算工具(RegulomeDB、CADD)及表观注释,研究进一步筛选出调控潜力最强的rs11102484。该位点位于1p13.2,具有多个组蛋白修饰峰、RegulomeDB评分2b和CADD评分9.64,被选为后续功能验证的核心位点。
rs11102484-G等位基因通过削弱ZNF263结合上调ST7L表达
rs11102484位于ST7L下游约112 kb处,eQTL分析显示G等位基因与ST7L表达升高显著相关(β=0.25,FDR=4.77×10⁻⁴)。双荧光素酶报告实验表明,包含C等位基因的片段具有沉默子活性(活性显著低于空载体),而G等位基因则使活性显著回升。CRISPRi介导的该区域扰动可上调ST7L表达并抑制细胞增殖。
3C实验证实,rs11102484所在区域与ST7L启动子存在物理相互作用,且相互作用频率在GG基因型细胞(PANC-1)中最低,在CC基因型细胞(BxPC-3)中最高,提示G等位基因减弱了远距离沉默子-启动子互作。
EMSA和ChIP-qPCR实验进一步揭示,转录抑制因子ZNF263优先结合C等位基因。rs11102484位于ZNF263的基序内,C→G突变破坏了基序匹配,导致ZNF263结合能力下降,从而解除了对ST7L的转录抑制。在CC基因型细胞中敲低ZNF263可上调ST7L表达并抑制增殖,验证了这一调控轴。
ST7L通过抑制AKT/β-catenin信号发挥抑癌功能
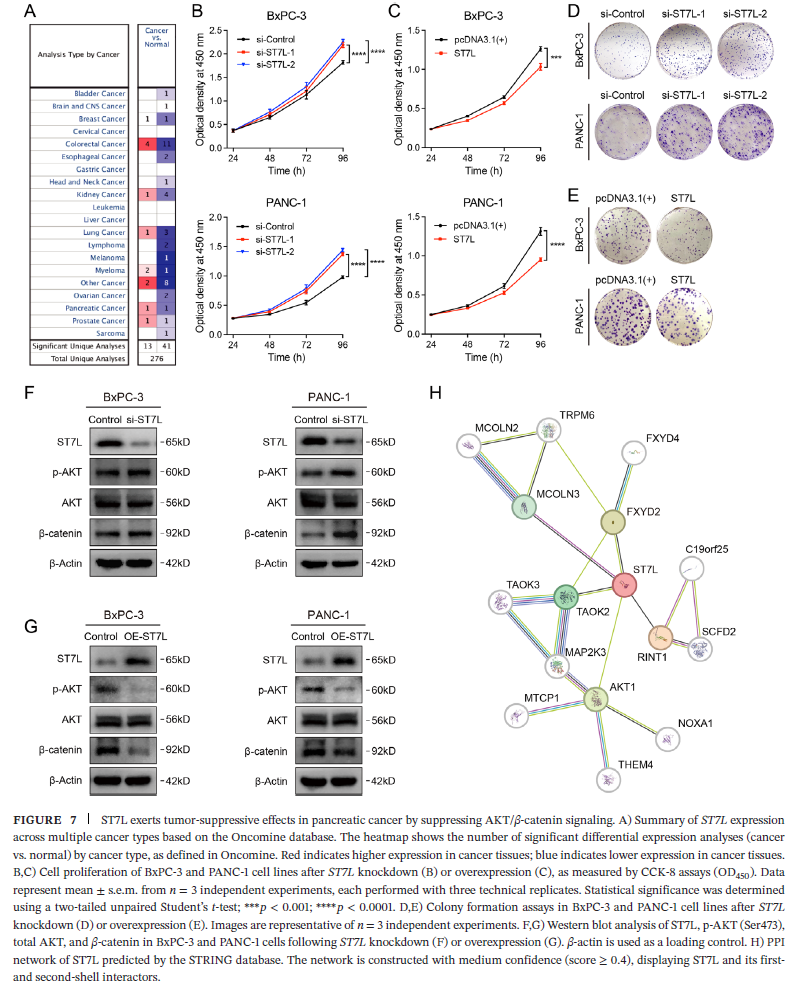
在三个独立的GEO数据集中,ST7L在胰腺癌组织中均显著下调。Oncomine数据库显示ST7L在多种癌症中表达降低。单细胞/单核RNA-seq数据表明,ST7L主要表达于上皮细胞和成纤维细胞,而在免疫细胞中表达较低。TCGA生存分析提示高表达ST7L的患者具有更长的总生存期和无进展生存期。
功能实验显示,ST7L敲低显著促进BxPC-3和PANC-1细胞的增殖和克隆形成,而ST7L过表达则产生相反效果。Western blot分析表明,ST7L敲低增加AKT Ser473磷酸化和β-catenin蛋白水平,而过表达ST7L则降低这两者的水平。这表明ST7L通过抑制AKT/β-catenin信号通路发挥肿瘤抑制作用。蛋白质相互作用网络预测ST7L可能还与TAOK2、MAP2K3、RINT1等分子互作,参与更广泛的信号调控。
讨论与展望
本研究通过大规模eQTL荟萃分析与GWAS的系统整合,绘制了胰腺癌遗传调控的全景图谱,优先筛选出82个功能性变异和15个易感基因。其中,rs11102484通过等位基因依赖的方式影响ZNF263结合,调节远距离沉默子-启动子染色质环互作,从而控制ST7L的表达水平。ST7L作为抑癌基因,通过抑制AKT/β-catenin信号通路减少细胞增殖,降低胰腺癌风险。该研究不仅为非编码风险变异的机制解析提供了范式,也为胰腺癌的遗传风险评估和靶向治疗(如激活ST7L表达或干扰ZNF263结合)提供了新的潜在策略。
技术服务列表
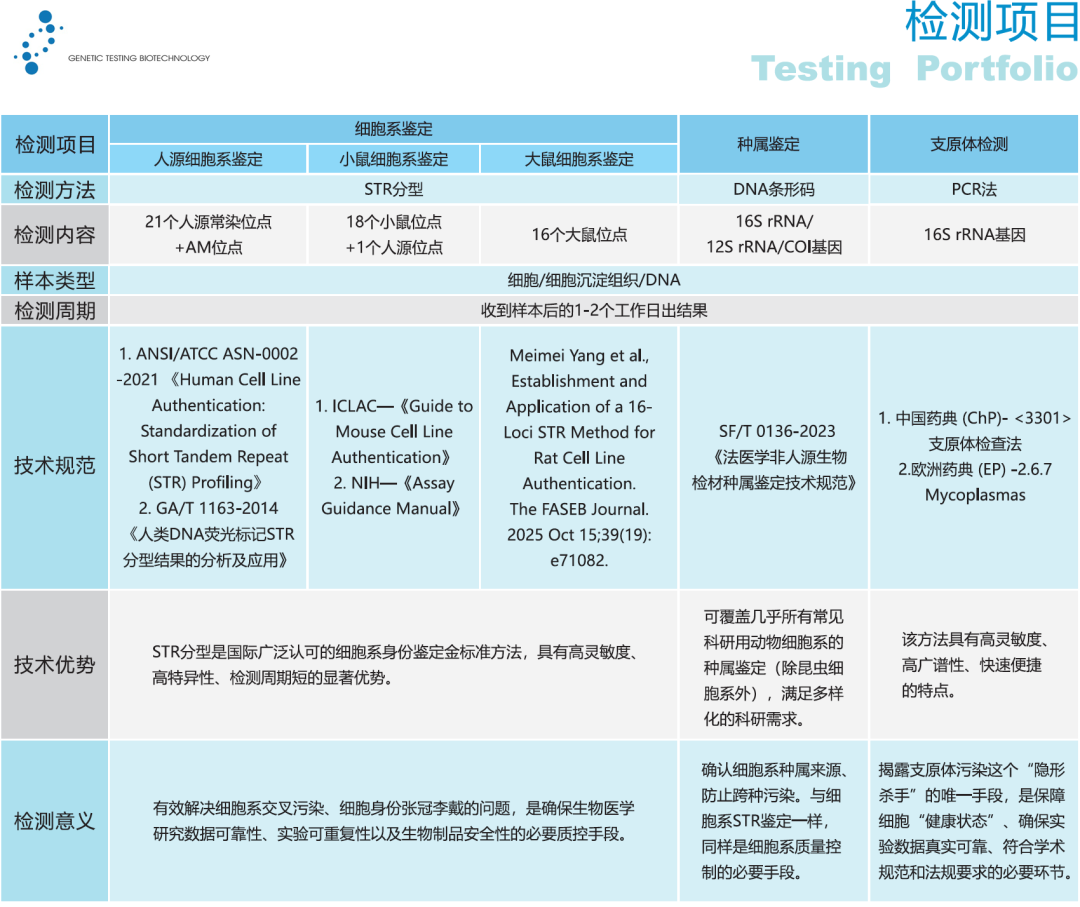
苏州鉴达(Genetic Testing Biotechnology, GTB)除提供细胞系STR鉴定服务外,还提供亲子鉴定业务。本公司的亲子鉴定业务包括常规的亲生血缘关系鉴定(三联体或二联体的亲权鉴定)、Y染色体鉴定、X染色体鉴定以及全同胞关系鉴定。苏州鉴达目前采用国际先进的STR检测技术,使用国际公认准确的ABI 3130 DNA遗传分析仪,亲子关系准确性高达99.99997%。如需了解更多细胞系STR鉴定及亲子鉴定的相关信息,可添加以下联系方式详询。
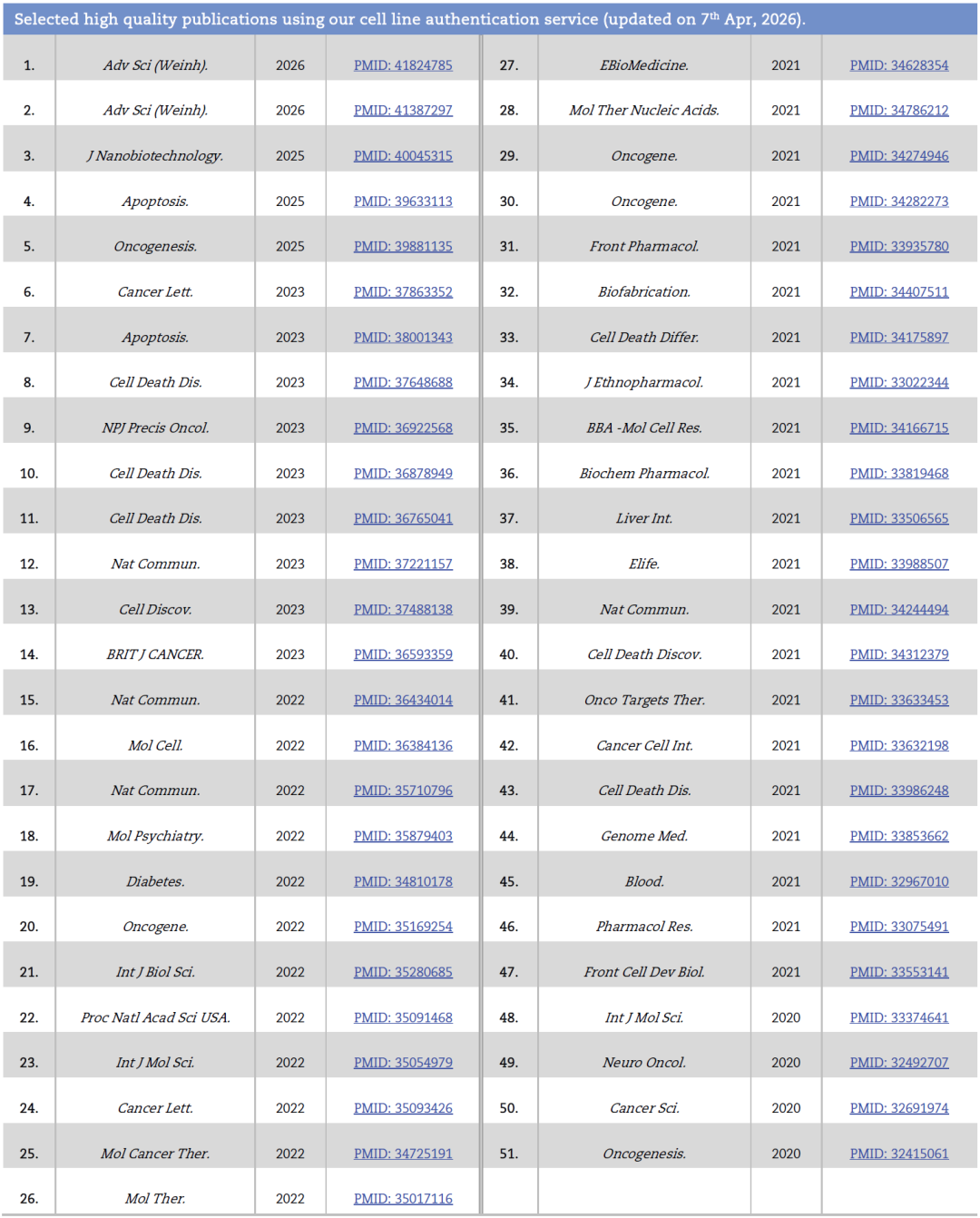
Selected high quality publications using our cell line authentication